保健食品中9种水溶性维生素的测定
1 范围
本方法规定了保健食品中维生素B1、维生素B2、泛酸、维生素B6、生物素、叶酸、维生素B12、烟酸、烟酰胺含量的液相色谱-串联质谱测定方法。
本方法适用于营养素补充剂类保健食品中维生素B1、维生素B2、泛酸、维生素B6、生物素、叶酸、维生素B12、烟酸、烟酰胺含量的测定。
2 原理
试样经水提取后,采用液相色谱-串联质谱仪检测,外标法定量。
3 试剂和材料
注:除非另有规定,本方法所用试剂均为分析纯,水为GB/T 6682规定的一级水。
3.1 试剂
3.1.1甲醇:质谱级。
3.1.2甲酸:质谱级。
3.1.3氨水:含量26%。
3.1.4冰醋酸。
3.1.5 浓盐酸。
3.1.6氨水(1+5):量取100 mL 氨水(3.1.3)缓慢倒入500 mL 水中,混匀。
3.1.7 盐酸(0.01 mol/L):吸取9 mL 浓盐酸(3.1.5),溶于1000 mL 水中。吸取该溶液50 mL,用水稀释并定容至500 mL。
3.1.8 0.1%甲酸水溶液:取甲酸1 mL用水稀释至1 000 mL,用滤膜(3.4)过滤后备用。
3.1.9 0.1%甲酸甲醇溶液:取甲酸1 mL用甲醇稀释至1000mL,用滤膜(3.4)过滤后备用。
3.2标准品
维生素B1(硫胺素盐酸盐)、维生素B2、泛酸(泛酸钙)、维生素B6(吡哆醇)、生物素、叶酸、维生素B12、烟酸、烟酰胺标准品的中文名称、英文名称、CAS登录号、分子式、相对分子量见附录A表A.1,纯度≥98%。
3.3标准溶液配制
3.3.1标准储备液(1 mg/mL)
3.3.1.1维生素B1标准储备液:称取维生素 B1标准品(3.2)0.1 g(精确至0.000 1 g),用 0.01 mol/L 盐酸(3.1.7)溶解并定容于100 mL棕色容量瓶中。
3.3.1.2维生素B2、生物素、叶酸标准储备液:分别称取生物素、叶酸标准品(3.2)0.1 g(精确至0.000 1 g),加入30 mL氨水(3.1.6)溶解,甲酸调节pH值至7.0后,用水转移并定容至100 mL棕色容量瓶中。
3.3.1.3 维生素B6、维生素B12、烟酸、烟酰胺、泛酸标准储备液:分别称取维生素B6、维生素B12、烟酸、烟酰胺和泛酸标准品(3.2)0.1 g(精确至0.000 1 g),用水溶解并定容至100 mL棕色容量瓶中。
3.3.2 空白基质溶液的配制
取空白试样按照试样制备方法(5.2)操作。
3.3.3基质标准工作液
3.3.3.1维生素B1基质标准工作液:准确吸取维生素B1标准储备液(3.3.1)适量,用空白基质溶液(3.3.2)将其稀释成含量分别为0.01 µg/mL、0.05 µg/mL、0.1 µg/mL、0.5 µg/mL、1 µg/mL的基质标准工作液。
3.3.3.2 8种维生素基质混合标准工作液:准确吸取维生素B2、泛酸、生物素、维生素B6、叶酸、维生素B12、烟酸、烟酰胺标准储备液(3.3.1)适量,用空白基质溶液将其稀释成含量分别为0.01 µg/mL、0.05 µg/mL、0.1 µg/mL、0.5 µg/mL、1 µg/mL的基质混合标准工作液。
注:操作过程应在避光环境下进行。
3.4微孔滤膜:0.22 µm,有机相。
4 仪器和设备
4.1 高效液相色谱-串联质谱仪:配有电喷雾离子源。
4.2 超声波清洗器。
4.3 分析天平:感量分别为0.01 g和0.000 1 g。
5 分析步骤
5.1试样制备
将20粒片剂或胶囊试样粉碎后混匀,液体试样混合均匀。
5.2试样提取
准确称取混合均匀的试样2g(精确至0.01 g)于50 mL棕色容量瓶中,加入40mL水,超声10 min,冷却至室温,用水定容至刻度,摇匀,上清液经微孔滤膜(3.4)过滤,供液相色谱-串联质谱仪测定。
注:操作过程应在避光环境下进行。
5.3 仪器参考条件
5.3.1 色谱条件
a)色谱柱: HSS T3柱,1.8 μm,100 mm×2.1 mm(内径),或性能相当者;
b)流动相:A为0.1%甲酸水溶液(3.1.8),B为0.1%甲酸甲醇溶液(3.1.9),洗脱梯度见表1;
c)流速:0.3 mL/min;
d)柱温:30℃;
e)进样量:2 μL。
表1 洗脱梯度
|
时间(min) |
流动相A(%) |
流动相B(%) |
|
0 |
99 |
1 |
|
3 |
99 |
1 |
|
5 |
5 |
95 |
|
8 |
50 |
50 |
|
10 |
99 |
1 |
|
15 |
99 |
1 |
5.3.2 质谱条件
a)电离方式:电喷雾正离子模式。
b)检测方式:多反应检测(MRM)。
c)雾化气压力:45psi。
d)离子喷雾电压:3500V。
e)干燥气温度:300℃。
f)干燥气流速:5 L/min。
g)定性离子对、定量离子、碎裂电压和碰撞能量见表2。
表2 水溶性维生素的定性离子对、定量离子、碎裂电压和碰撞能量
|
中文名称 |
母离子 (m/z) |
子离子 (m/z) |
碎裂电压 ( V) |
碰撞能量 (eV) |
|
维生素B1 |
265.1 |
122.2*;144.1 |
100 |
15;15 |
|
维生素B2 |
377.1 |
243.1*;172.2 |
135 |
25;32 |
|
泛酸 |
220.2 |
90.1*;184.2 |
100 |
10;20 |
|
维生素B6 |
170.2 |
152.1*;134.1 |
100 |
12;22 |
|
生物素 |
245.1 |
227.1*;97.1 |
100 |
12;22 |
|
叶酸 |
442.1 |
295.1*;176.2 |
100 |
10;40 |
|
维生素B12 |
679.4 |
147.2*;359.1 |
200 |
20;40 |
|
烟酸 |
124.1 |
80.1*;78.1 |
100 |
28;32 |
|
烟酰胺 |
123.1 |
80.1*;53.1 |
100 |
5;5 |
* :定量离子
5.4 定性测定
按照上述条件测定试样和混合标准工作液,如果试样中的质量色谱峰保留时间与混合标准工作液中的某种组分一致(变化范围在±2.5%之内);试样中定性离子对的相对丰度与浓度相当混合标准工作液的相对丰度一致,相对丰度偏差不超过表3规定的范围,则可判定为试样中存在该组分。
表3 定性确证时相对离子丰度的最大允许偏差
|
相对离子丰度(%) |
>50 |
>20~50 |
>10~20 |
≤10 |
|
允许的最大偏差(%) |
± 20 |
± 25 |
± 30 |
± 50 |
5.5 定量测定
5.5.1 标准曲线的制作
将基质标准工作液(3.3.3)分别按仪器参考条件(5.3)进行测定,得到相应的标准溶液的色谱峰面积。以基质标准工作液的浓度为横坐标,以色谱峰的峰面积为纵坐标,绘制标准曲线。
5.5.2 试样溶液的测定
将试样溶液(5.2)按仪器参考条件(5.3)进行测定,得到相应的样品溶液的色谱峰面积。根据标准曲线得到待测液中组分的浓度,平行测定次数不少于两次;试样待测液响应值若低于标准曲线线性范围,应取5.2中试样提取续滤液进行分析;试样待测液响应值若超出标准曲线线性范围,应用水稀释后进行分析。
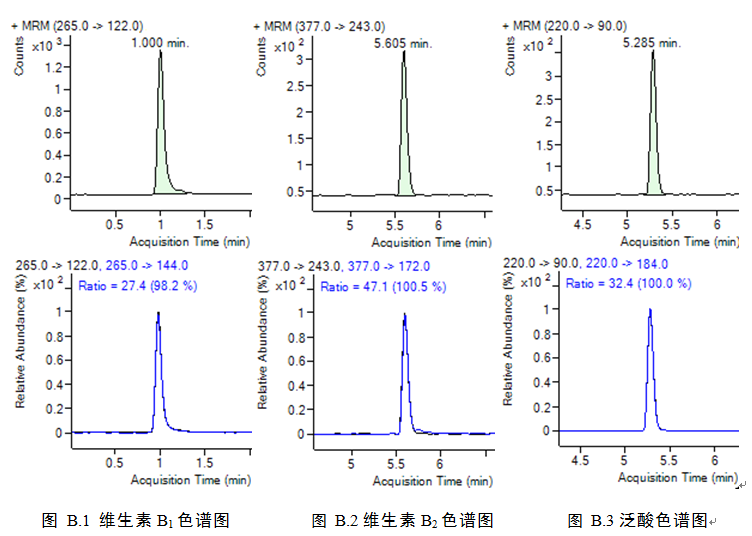
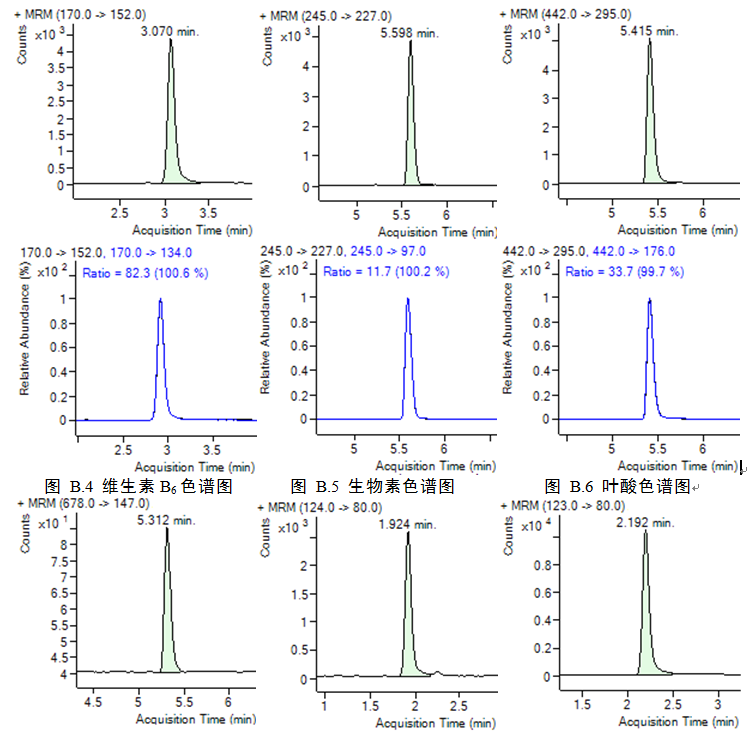
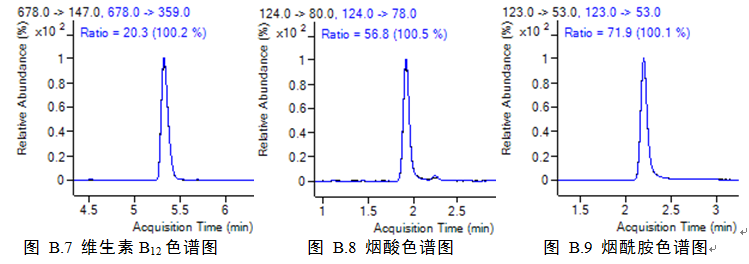
标准品液相色谱图参见附录B的图B.1-B.9。
6 结果计算
结果按式(1)计算:
…………………………………………(1)
式中:
X—试样中某种组分的含量,单位为微克每百克(μg/100g);
c—由标准曲线得出的样液中某种组分的浓度,单位为微克每毫升(μg/mL);
V—试样溶液定容体积,单位为毫升(mL);
m—试样称取的质量,单位为克(g);
计算结果以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留三位有效数字。
7 精密度
在重复条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
8 其他
当称样量为2.00 g,定容体积为50 mL时,维生素B1、维生素B6、叶酸检出限为2.5μg/100g,定量限为10μg/100g;维生素B2、泛酸、烟酸、烟酰胺检出限为5μg/100g,定量限为15μg/100g;生物素、维生素B12检出限为7.5μg/100g,定量限为25μg/100g。
附录A
水溶性维生素标准品信息
表A.1 水溶性维生素标准品的中文名称、英文名称、CAS登录号、分子式、相对分子量
|
序号 |
中文名称 |
英文名称 |
CAS登录号 |
分子式 |
相对分子量 |
|
1 |
维生素B1 |
Thiamine |
59-43-8 |
C12H17ClN4OS |
264.35 |
|
2 |
维生素B2 |
Riboflavin |
83-88-5 |
C17H20N4O6 |
376.37 |
|
3 |
泛酸 |
Pantothenic Acid |
137-08-6 |
C9H17NO5 |
219.23 |
|
4 |
维生素B6 |
Pyridoxine |
65-23-6 |
C8H11NO3 |
169.18 |
|
5 |
生物素 |
Biotin |
58-85-5 |
C10H16N2O3S |
244.30 |
|
6 |
叶酸 |
Folic Acid |
53-30-3 |
C19H19N7O6 |
441.40 |
|
7 |
维生素B12 |
Vitamin B12 |
200-680-0 |
C63H88CoN14O14P |
1355.37 |
|
8 |
烟酸 |
Nicotinic Acid |
C6H5NO2 |
123.11 |
|
|
9 |
烟酰胺 |
Nicotinamide |
98-92-0 |
C6H6N2O |
122.13 |
附录B
水溶性维生素标准品色谱图
本方法负责起草单位:中国食品药品检定研究院。
验证单位:山东省食品药品检验研究院、武汉市食品化妆品检验所、天津市药品检验所、中国医学科学院药物研究所、厦门市药品检验研究院。
主要起草人:宁霄、金绍明、曹进、梁瑞强、李启艳、江小明



